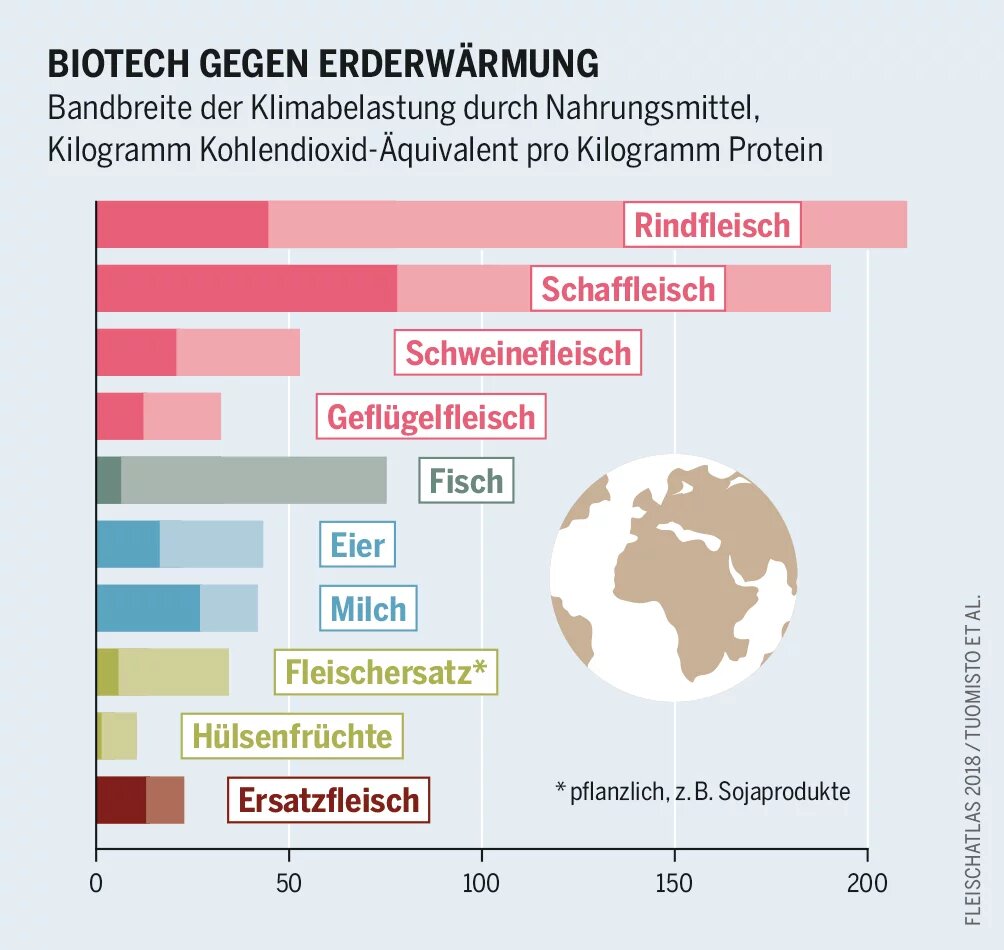
Mit In-vitro-Fleisch wollen Biotechnologen das Bedürfnis der Welt nach immer mehr tierischem Protein stillen. Während die Kosten sinken, steigen die Kenntnisse über den Aufwand und die Risiken der Produktion.
Im Juli 2016 schaltete ein israelisches Start-up namens SuperMeat eine Crowdfunding-Kampagne im Internet. Es warb für die Finanzierung eines Gerätes, für das noch nicht einmal ein Design oder ein Bauplan vorlagen – einen Bioreaktor für den Hausgebrauch, der Hühnerfleisch produziert. Die Maschine, so warb ein Video, lasse sich in Supermärkten, Restaurants oder sogar in Privathaushalten aufstellen. Nach nicht einmal zwei Monaten war die Zielmarke von 100.000 Dollar erreicht. Inzwischen hat SuperMeat den Betrag auf eine halbe Million Dollar erhöht. Noch bevor der Schritt von der Vision zum Plan gemacht war, fanden sich genügend Leute, die das Verfahren finanzieren.
Das zeigt, wie faszinierend die Idee für viele sein muss, Fleisch zu produzieren, ohne dass dafür ein Tier leiden und sterben muss. „Cultured meat“, „clean meat“ oder zu deutsch „In-vitro-Fleisch“ sind die Schlagworte, mit denen junge Biotechnologie-Firmen aus den USA, den Niederlanden und eben aus Israel derzeit um Investorinnen und Investoren werben. Science-Fiction ist das nicht mehr. Laut den Unternehmen ist es nur noch ein kleiner Schritt, bis Hühnchen-Nuggets, Fischstäbchen oder Burger-Pattys aus der Petrischale in den Supermärkten liegen.
Nach Herzklappen und Hautgewebe kommt jetzt das Steak
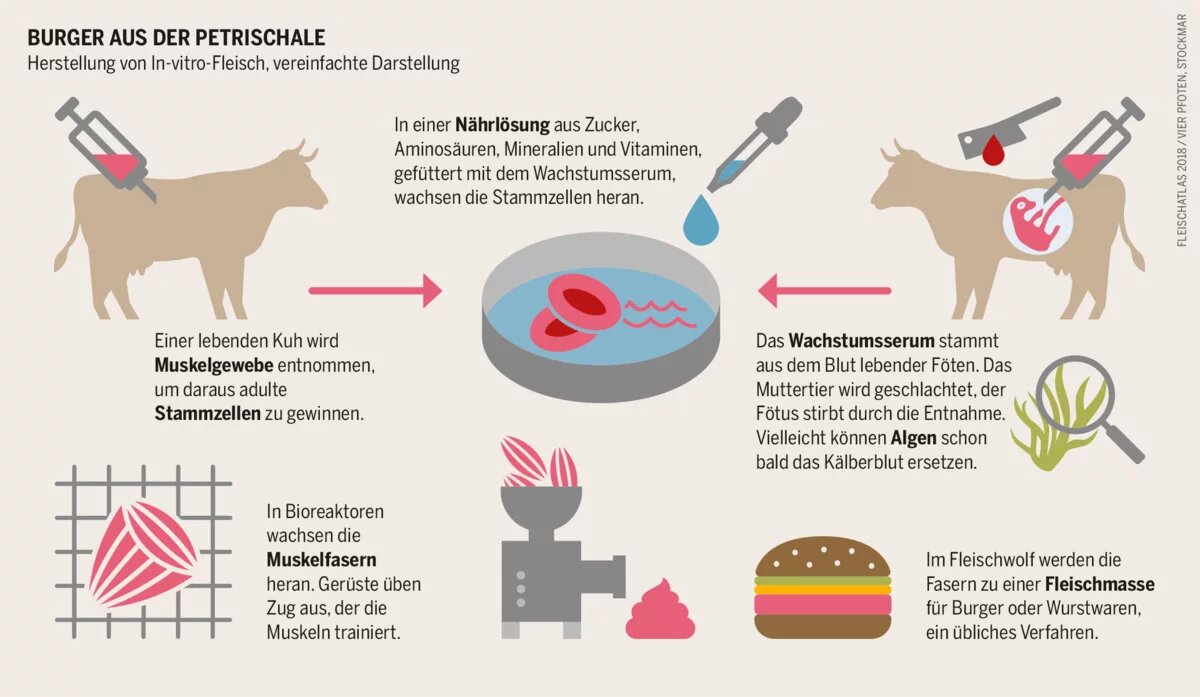
Die eigentliche Technologie dahinter ist erprobt. Schon seit Jahren werden Herzklappen, Hautgewebe oder Ohrmuscheln im Labor gezüchtet. Also sollte das auch bei Steaks und Schnitzel klappen, sagten sich die Forscherinnen und Forscher. Die Erzeugung basiert auf Techniken der Zellvervielfältigung und Gewebezüchtung. Sie verläuft wie das sogenannte „Tissue Engineering“, ganz ähnlich der In-vitro-Produktion von embryonalen Stammzellen. Diese Zellen können sich unendlich oft teilen, wodurch immer neue, identische Zellen entstehen – theoretisch ein grenzenloses Wachstum. Durch eine Biopsie werden einem lebenden Tier Muskelstammzellen entnommen. Diese Zellen werden in einem Nährmedium kultiviert und vermehren sich. Billionen von Stammzellen bilden anschließend Muskelzellen, die zu Muskel- und Fleischfasern zusammenwachsen. Das ist eine Sache von Wochen. Um einen Hamburger zu formen, braucht man etwa 20.000 solcher Fasern.
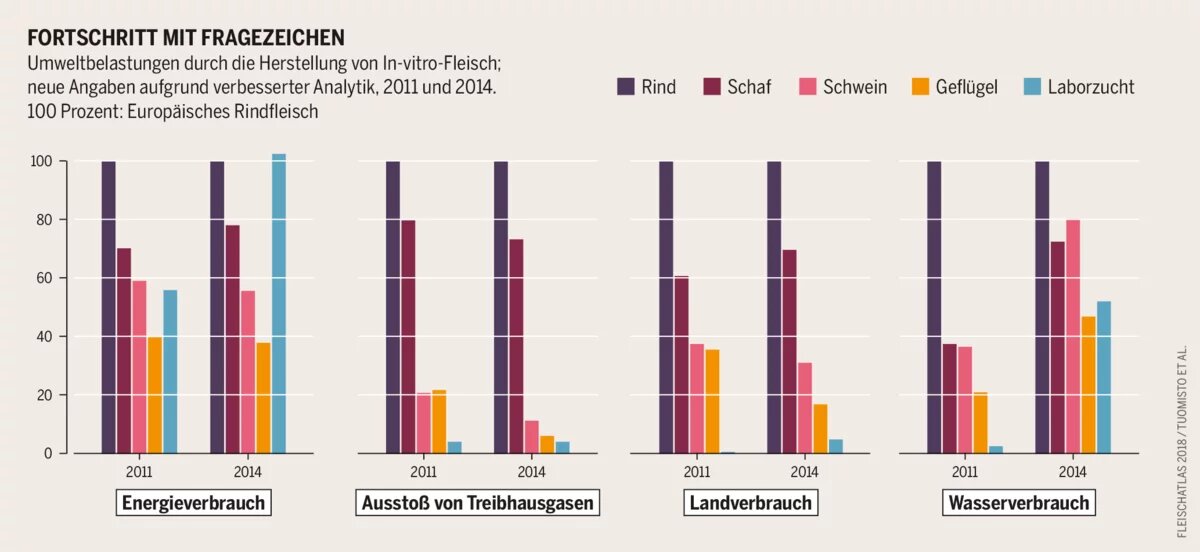
Die In-vitro-Metzger haben den moralischen Vorteil im Auge, aber sie argumentieren auch ökologisch. Fleisch aus Fabriken, die eher Raffinerien oder Chemieanlagen entsprechen, machen mit der Massentierhaltung Schluss. Die Ernährungs- und Landwirtschaftsorganisation der Vereinten Nationen erwartet, dass sich bis 2050 die weltweite Fleischproduktion auf 465 Millionen Tonnen jährlich nahezu verdoppelt. Bis dahin wird es wohl noch immer viele Fleischesser geben. Daher die Argumente: Kunstfleisch aus dem Bioreaktor sei nachhaltiger herzustellen. Der Energieverbrauch lasse sich um bis zu 45 Prozent gegenüber der konventionellen Fleischherstellung zurückdrehen. Die Emissionen von Treibhausgasen, der Flächen- und der Wasserverbrauch sänken sogar um über 95 Prozent. Aber solche Angaben haben schon revidiert werden müssen, und der Energieverbrauch der Bioreaktoren könnte deutlich höher sein als der der industriellen Geflügel- und Schweinehaltung.
1997 erhielt der niederländische Forscher Willem van Eelen das erste Patent zur Herstellung von In-vitro-Fleisch. 1998 folgten Patente in den USA. Einige wenige Biotech-Firmen könnten nun den Markt unter sich aufteilen. 2013 ging der niederländische Biologe Mark Post mit dem ersten künstlichen Burger an die Öffentlichkeit und lud zur Verkostung. Die Kritik war wohlwollend, der Preis des Gerichts exorbitant. Die ganze Entwicklung eingerechnet, kostete der erste In-vitro-Burger rund 330.000 US-Dollar. Als Finanzier stand der Google-Gründer Sergey Brin hinter dem Projekt.
Wie können wir Fleisch wachsen lassen?
Eine der größten Herausforderungen für die Biotechnologen ist derweil das Nährmedium, in dem das Fleisch wächst. Bislang ist es Kälberserum, das aus den Föten geschlachteter schwangerer Kühe gewonnen wird und voller Wachstumshormone steckt. Aus tierethischer Sicht ist dies problematisch, weil wahrscheinlich auch die Föten zu diesem Zeitpunkt bereits Leid empfinden. In Deutschland ist seit Mai 2017 die Schlachtung von tragenden Tieren im letzten Drittel der Schwangerschaft untersagt.
SuperMeat gibt an, bereits auf rein pflanzlichen Nährböden Zellen vermehrt zu haben. Noch immer erfordert die Herstellung auch die Zugabe von Antibiotika, denn Bakterien machen auch vor künstlichem Fleisch nicht halt. Die Forscher beschäftigen sich derzeit mit der komplexen Struktur ihres Objekts, um dem Original noch näher zu kommen. Fleisch besteht nicht nur aus Muskelfasern, sie werden von Colagenen gehalten und von Fettgewebe umhüllt, das auch für den Geschmack verantwortlich ist.
Einige Unternehmen haben Verfahren entwickelt, um Fleisch aus Zellen pflanzlicher Herkunft zu gewinnen. Mitte 2017 geriet die US-Firma Impossible Foods mit ihrem fleischfreien Burger in die Kritik. Ihr Geschmacksträger stammte aus einer genetisch veränderten Hefe, die keine Zulassung erhalten hatte. Umweltorganisationen kritisieren, dass die gentechnischen Verfahren für die In-vitro-Fleischproduktion nicht transparent sind. Dennoch – oder gerade deshalb – haben die Technologinnen und Technologen in den vergangenen vier Jahren deutliche wirtschaftliche Fortschritte gemacht. Die Kosten von Mark Posts Burger, heißt es, lägen inzwischen bei nur noch elf US-Dollar.